Polonium (Po), unsur logam radioaktif, abu-abu keperakan atau hitam dari kelompok oksigen (Grup 16 [VIa] dalam tabel periodik). Unsur pertama yang ditemukan oleh analisis radiokimia, polonium ditemukan pada tahun 1898 oleh Pierre dan Marie Curie, yang sedang menyelidiki radioaktivitas bijih uranium tertentu. Radioaktivitas yang sangat kuat yang tidak dapat dikaitkan dengan uranium dianggap berasal dari unsur baru, dinamai oleh mereka setelah tanah air Marie Curie, Polandia. Penemuan ini diumumkan pada Juli 1898. Polonium sangat langka, bahkan dalam bijih uranium: 1.000 ton bijih harus diproses untuk mendapatkan 40 miligram polonium. Kelimpahannya di kerak bumi adalah sekitar satu bagian dalam 10 15. Ini terjadi di alam sebagai produk peluruhan radioaktif uranium, thorium, dan actinium. Waktu paruh isotopnya berkisar dari sepersekian detik hingga 103 tahun; isotop alami polonium yang paling umum, polonium-210, memiliki paruh 138,4 hari.
Polonium biasanya diisolasi dari produk sampingan dari ekstraksi radium dari mineral uranium. Dalam isolasi kimia, bijih uranium diolah dengan asam klorida, dan larutan yang dihasilkan dipanaskan dengan hidrogen sulfida untuk mengendapkan polonium monosulfida, PoS, bersama dengan sulfida logam lainnya, seperti bismut, Bi 2 S 3, yang menyerupai polonium monosulfida erat dalam perilaku kimia, meskipun kurang larut. Karena perbedaan kelarutan, presipitasi parsial berulang dari campuran sulfida mengkonsentrasikan polonium dalam fraksi yang lebih mudah larut, sedangkan bismut terakumulasi dalam bagian-bagian yang kurang larut. Perbedaan dalam kelarutan kecil, namun, dan prosesnya harus diulang berkali-kali untuk mencapai pemisahan yang lengkap. Pemurnian dicapai dengan deposisi elektrolitik. Ini dapat diproduksi secara artifisial dengan membombardir bismut atau timah dengan neutron atau dengan partikel bermuatan dipercepat.
Secara kimia, polonium menyerupai elemen telurium dan bismut. Dua modifikasi polonium diketahui, bentuk α dan β, keduanya stabil pada suhu kamar dan memiliki karakteristik logam. Fakta bahwa konduktivitas listriknya berkurang ketika suhu meningkat menempatkan polonium di antara logam daripada metaloid atau bukan logam.
Karena polonium sangat radioaktif - ia hancur menjadi isotop timbal yang stabil dengan memancarkan sinar alpha, yang merupakan aliran partikel bermuatan positif - ia harus ditangani dengan sangat hati-hati. Ketika terkandung dalam zat-zat seperti kertas emas, yang mencegah radiasi alfa dari melarikan diri, polonium digunakan secara industri untuk menghilangkan listrik statis yang dihasilkan oleh proses seperti kertas bergulir, pembuatan lembaran plastik, dan pemintalan serat sintetis. Ini juga digunakan pada sikat untuk menghilangkan debu dari film fotografi dan dalam fisika nuklir sebagai sumber radiasi alfa. Campuran polonium dengan berilium atau elemen ringan lainnya digunakan sebagai sumber neutron.
Properti Elemen
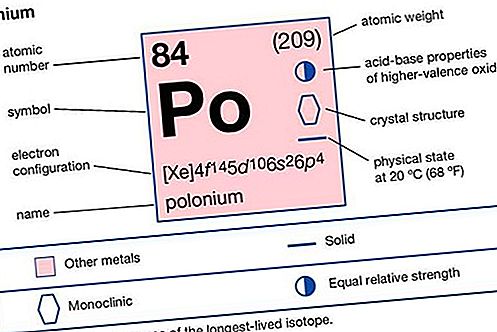
| nomor atom | 84 |
|---|---|
| berat atom | 210 |
| titik lebur | 254 ° C (489 ° F) |
| titik didih | 962 ° C (1.764 ° F) |
| massa jenis | 9,4 g / cm 3 |
| keadaan oksidasi | −2, +2, +3 (?), +4, +6 |
| konfigurasi elektron. | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 6s 2 6p 4 |


![Film Gladiator oleh Scott [2000] Film Gladiator oleh Scott [2000]](https://images.thetopknowledge.com/img/entertainment-pop-culture/1/gladiator-film-scott-2000.jpg)










