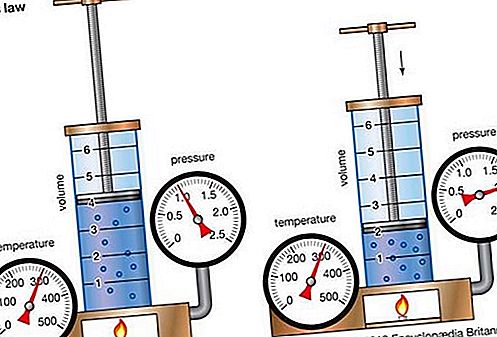
Hukum Boyle, juga disebut hukum Mariotte, hubungan tentang kompresi dan ekspansi gas pada suhu konstan. Hubungan empiris ini, yang dirumuskan oleh fisikawan Robert Boyle pada tahun 1662, menyatakan bahwa tekanan (p) dari jumlah gas yang diberikan bervariasi berbanding terbalik dengan volumenya (v) pada suhu konstan; yaitu, dalam bentuk persamaan, pv = k, sebuah konstanta. Hubungan itu juga ditemukan oleh fisikawan Prancis Edme Mariotte (1676).
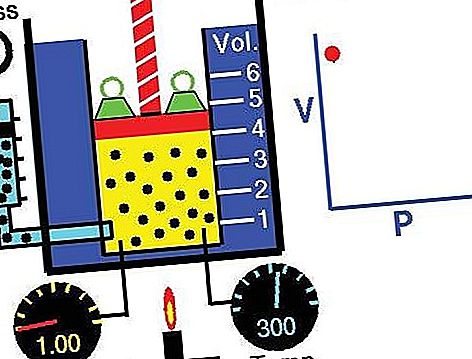
Hukum dapat diturunkan dari teori kinetik gas dengan asumsi gas (ideal) sempurna (lihat gas sempurna). Gas nyata mematuhi hukum Boyle pada tekanan yang cukup rendah, meskipun pv produk umumnya sedikit menurun pada tekanan yang lebih tinggi, di mana gas mulai menyimpang dari perilaku ideal.