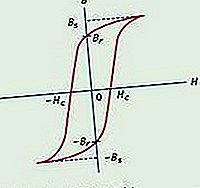
Elektrolisa, proses dimana arus listrik dilewatkan melalui suatu zat untuk menghasilkan perubahan kimia. Perubahan kimia adalah perubahan substansi yang kehilangan atau memperoleh elektron (oksidasi atau reduksi). Proses ini dilakukan dalam sel elektrolitik, suatu alat yang terdiri dari elektroda positif dan negatif yang dipisah dan dicelupkan ke dalam larutan yang mengandung ion bermuatan positif dan negatif. Zat yang akan ditransformasikan dapat membentuk elektroda, dapat merupakan larutan, atau dapat larut dalam larutan. Arus listrik (yaitu, elektron) masuk melalui elektroda bermuatan negatif (katoda); komponen larutan bergerak ke elektroda ini, bergabung dengan elektron, dan diubah (dikurangi). Produk dapat berupa elemen netral atau molekul baru. Komponen larutan juga bergerak ke elektroda lain (anoda), melepaskan elektronnya, dan diubah (teroksidasi) menjadi elemen netral atau molekul baru. Jika substansi yang ditransformasikan adalah elektroda, reaksinya sering kali adalah di mana elektroda larut dengan melepaskan elektron.

industri kimia: proses elektrolitik
Kemudian pada abad ke-19 pengembangan pembangkit tenaga listrik memungkinkan industri elektrokimia. Ini tidak dapat diidentifikasi dengan jelas
Elektrolisis digunakan secara luas dalam proses metalurgi, seperti dalam ekstraksi (electrowinning) atau pemurnian (electrorefining) logam dari bijih atau senyawa dan dalam pengendapan logam dari larutan (electroplating). Natrium logam dan gas klor dihasilkan oleh elektrolisis natrium klorida cair; elektrolisis larutan berair natrium klorida menghasilkan natrium hidroksida dan gas klor. Hidrogen dan oksigen dihasilkan oleh elektrolisis air.



![Pertempuran Tripoli Harbour Perang Tripoli Kedua [1804] Pertempuran Tripoli Harbour Perang Tripoli Kedua [1804]](https://images.thetopknowledge.com/img/world-history/4/second-battle-tripoli-harbor-tripolitan-war-1804.jpg)