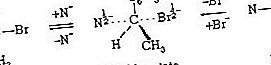Teori Lewis, generalisasi tentang asam dan basa yang diperkenalkan pada tahun 1923 oleh ahli kimia AS Gilbert N. Lewis, di mana asam dianggap sebagai senyawa apa pun yang, dalam reaksi kimia, mampu melekatkan dirinya pada pasangan elektron yang tidak terbagi dalam elektron lain dalam molekul lain.. Molekul dengan pasangan elektron yang tersedia disebut basa. Reaksi antara asam dan basa (netralisasi) menghasilkan pembentukan senyawa tambahan, di mana pasangan elektron yang membentuk ikatan kimia hanya berasal dari satu reaktan. Termasuk dalam definisi asam Lewis adalah ion logam; oksida unsur nonlogam tertentu, seperti sulfur, fosfor, dan nitrogen; zat yang mampu menyumbangkan ion atau proton hidrogen; dan senyawa padat tertentu, seperti aluminium klorida, boron trifluorida, silika, dan alumina.

reaksi kimia: Teori Lewis
Teori asam dan basa yang masih lebih luas diusulkan oleh ahli kimia fisik Amerika Gilbert Newton Lewis. Dalam teori Lewis,
Dalam praktiknya, zat yang dianggap asam menurut definisi Lewis, selain yang terkait dengan ion hidrogen dan proton, secara khusus disebut sebagai asam Lewis. Basa Lewis termasuk amonia dan turunan organiknya, oksida dari logam alkali dan alkali tanah, dan sebagian besar atom dan molekul dengan muatan listrik negatif (anion).