Penambahan nukleofil karbon
Berbagai macam nukleofil karbon menambah aldehida, dan reaksi semacam itu sangat penting dalam kimia organik sintetis karena produk ini merupakan kombinasi dari dua kerangka karbon. Kimiawan organik telah mampu mengumpulkan hampir semua kerangka karbon, betapa pun rumitnya, dengan menggunakan reaksi-reaksi ini secara cerdik. Salah satu yang tertua dan paling penting adalah penambahan reagen Grignard (RMgX, di mana X adalah atom halogen). Kimiawan Perancis Victor Grignard memenangkan Hadiah Nobel 1912 dalam bidang kimia atas penemuan reagen ini dan reaksi mereka.
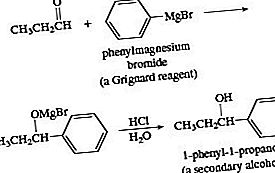
Penambahan pereaksi Grignard pada aldehida diikuti dengan pengasaman dalam asam berair menghasilkan alkohol. Penambahan formaldehyde menghasilkan alkohol primer. Penambahan aldehida selain formaldehida menghasilkan alkohol sekunder.
Nukleofil karbon lainnya adalah ion sianida, CN -, yang bereaksi dengan aldehida untuk menghasilkan, setelah pengasaman, sianohidrin, senyawa yang mengandung gugus OH dan CN pada atom karbon yang sama.
Benzaldehyde cyanohydrin (mandelonitrile) memberikan contoh yang menarik dari mekanisme pertahanan kimia di dunia biologis. Zat ini disintesis oleh kaki seribu (Apheloria corrugata) dan disimpan dalam kelenjar khusus. Ketika kaki seribu terancam, sianohidrin dikeluarkan dari kelenjar penyimpanannya dan mengalami disosiasi yang dikatalisis oleh enzim untuk menghasilkan hidrogen sianida (HCN). Kaki seribu kemudian melepaskan gas HCN ke lingkungan sekitarnya untuk menangkal predator. Jumlah HCN yang dipancarkan oleh satu kaki seribu cukup untuk membunuh tikus kecil. Mandelonitrile juga ditemukan dalam almond pahit dan lubang persik. Fungsinya di sana tidak diketahui.
Reaksi penting lainnya dalam kategori ini termasuk reaksi Knoevenagel, di mana karbon nukleofil adalah ester dengan setidaknya satu α-hidrogen. Dengan adanya basa kuat, ester kehilangan α-hidrogen untuk menghasilkan karbon bermuatan negatif yang kemudian menambah karbon karbonil dari aldehida. Pengasaman diikuti dengan hilangnya molekul air menghasilkan ester tak jenuh α, β.
Reaksi adisi lain yang melibatkan nukleofil karbon adalah reaksi Wittig, di mana aldehida bereaksi dengan fosforan (juga disebut fosfor ylide), untuk menghasilkan senyawa yang mengandung ikatan rangkap karbon-karbon. Hasil dari reaksi Wittig adalah penggantian oksigen karbonil dari aldehida oleh gugus karbon yang terikat pada fosfor. Ahli kimia Jerman Georg Wittig membagikan Hadiah Nobel 1979 dalam bidang kimia untuk penemuan reaksi ini dan pengembangan penggunaannya dalam kimia organik sintetis.
Senyawa yang mengandung gugus trimetilsilil (iSiMe 3, di mana Me adalah gugus metil, ―CH 3) dan atom litium (Li) pada atom karbon yang sama bereaksi dengan aldehida dalam reaksi Peterson yang disebut untuk menghasilkan produk yang sama yang akan diperoleh dengan reaksi Wittig yang sesuai.
Perpindahan di α-karbon
α-Halogenasi
Suatu α-hidrogen aldehida dapat diganti dengan atom klor (Cl), brom (Br), atau iodin (I) ketika senyawa diperlakukan masing-masing dengan Cl 2, Br 2, atau I 2, baik tanpa katalis. atau di hadapan katalis asam.
Reaksi dapat dengan mudah dihentikan setelah hanya satu atom halogen yang ditambahkan. α-Halogenasi sebenarnya terjadi pada bentuk enol (lihat di atas Properti aldehida: Tautomerisme) dari aldehida daripada pada aldehida itu sendiri. Reaksi yang sama terjadi jika basa ditambahkan, tetapi kemudian tidak dapat dihentikan sampai semua α-halogen yang terikat pada karbon yang sama telah digantikan oleh atom halogen. Jika ada tiga α-hidrogen pada karbon yang sama, reaksi berjalan selangkah lebih maju, menghasilkan pembelahan ion X 3 C - (di mana X adalah halogen) dan pembentukan garam dari asam karboksilat.

Reaksi ini disebut reaksi haloform, karena ion X 3 C - bereaksi dengan air atau asam lain yang ada dalam sistem untuk menghasilkan senyawa dalam bentuk X 3 CH, yang disebut haloform (misalnya, CHCl 3 disebut kloroform).