Berilium (Be), sebelumnya (sampai 1957) glukinium, unsur kimia, anggota paling ringan dari logam alkali tanah Grup 2 (IIa) dari tabel periodik, digunakan dalam metalurgi sebagai bahan pengeras dan dalam banyak aplikasi luar angkasa dan nuklir..
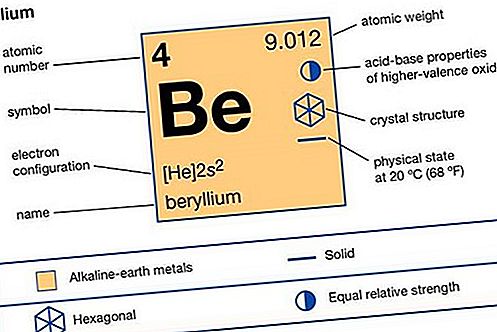

logam alkali-tanah
Unsur-unsurnya adalah berilium (Be), magnesium (Mg), kalsium (Ca), strontium (Sr), barium (Ba), dan radium (Ra).
Properti Elemen
| nomor atom | 4 |
|---|---|
| berat atom | 9.0122 |
| titik lebur | 1.287 ° C (2.349 ° F) |
| titik didih | 2.471 ° C (4.480 ° F) |
| berat jenis | 1.85 pada 20 ° C (68 ° F) |
| keadaan oksidasi | +2 |
| konfigurasi elektron | 1s 2 2s 2 |
Kejadian, properti, dan penggunaan
Berilium adalah logam baja abu-abu yang cukup rapuh pada suhu kamar, dan sifat kimianya agak mirip dengan aluminium. Itu tidak terjadi secara gratis di alam. Berilium ditemukan dalam beryl dan zamrud, mineral yang dikenal orang Mesir kuno. Meskipun telah lama diduga bahwa kedua mineral itu serupa, konfirmasi kimiawi tentang hal ini tidak terjadi sampai akhir abad ke-18. Zamrud sekarang dikenal sebagai varietas beryl hijau. Berilium ditemukan (1798) sebagai oksida oleh kimiawan Perancis Nicolas-Louis Vauquelin dalam beryl dan dalam zamrud dan diisolasi (1828) sebagai logam secara independen oleh kimiawan Jerman Friedrich Wöhler dan kimiawan Perancis Antoine AB Bussy oleh pengurangan klorida dengan kalium. Berilium tersebar luas di kerak bumi dan diperkirakan terjadi di batuan beku Bumi hingga 0,0002 persen. Kelimpahan kosmiknya adalah 20 pada skala di mana silikon, standarnya, adalah 1.000.000. Amerika Serikat memiliki sekitar 60 persen dari berilium dunia dan sejauh ini merupakan produsen berilium terbesar; negara penghasil utama lainnya termasuk Cina, Mozambik, dan Brasil.
Ada sekitar 30 mineral yang dikenali yang mengandung berilium, termasuk beril (Al 2 Be 3 Si 6 O 18, berilium aluminium silikat), bertrandit (Be 4 Si 2 O 7 (OH) 2, berilium silikat), fenakit (Be 2 SiO 4), dan chrysoberyl (BeAl 2 O 4). (Bentuk beril, zamrud dan aquamarine yang berharga, memiliki komposisi yang mendekati yang diberikan di atas, tetapi bijih industri mengandung lebih sedikit berilium; sebagian besar beril diperoleh sebagai produk sampingan dari operasi penambangan lainnya, dengan kristal yang lebih besar diambil dengan tangan.) Beryl dan bertrandit telah ditemukan dalam jumlah yang cukup untuk membentuk bijih komersial dari mana berilium hidroksida atau berilium oksida diproduksi secara industri. Ekstraksi berilium diperumit oleh fakta bahwa berilium adalah unsur kecil di sebagian besar bijih (5 persen massa bahkan dalam beril murni, kurang dari 1 persen massa bertrandit) dan terikat erat dengan oksigen. Pengobatan dengan asam, pemanggangan dengan fluorida kompleks, dan ekstraksi cair-cair semuanya telah digunakan untuk memekatkan berilium dalam bentuk hidroksida-nya. Hidroksida diubah menjadi fluorida melalui amonium berilium fluorida dan kemudian dipanaskan dengan magnesium untuk membentuk unsur berilium. Sebagai alternatif, hidroksida dapat dipanaskan untuk membentuk oksida, yang selanjutnya dapat diolah dengan karbon dan klor untuk membentuk berilium klorida; elektrolisis lelehan klorida kemudian digunakan untuk menghasilkan logam. Unsur ini dimurnikan dengan pencairan vakum.
Berilium adalah satu-satunya logam ringan yang stabil dengan titik leleh yang relatif tinggi. Meskipun mudah diserang oleh alkali dan asam nonoksidasi, berilium dengan cepat membentuk lapisan permukaan oksida yang melekat yang melindungi logam dari oksidasi udara lebih lanjut dalam kondisi normal. Sifat-sifat kimia ini, ditambah dengan konduktivitas listriknya yang sangat baik, kapasitas dan konduktivitas panas yang tinggi, sifat mekanik yang baik pada suhu yang tinggi, dan modulus elastisitas yang sangat tinggi (sepertiga lebih besar dari baja), membuatnya berharga untuk aplikasi struktural dan termal. Stabilitas dimensi Berilium dan kemampuannya untuk mengambil polesan tinggi telah membuatnya berguna untuk cermin dan penutup kamera dalam aplikasi ruang, militer, dan medis dan dalam pembuatan semikonduktor. Karena berat atomnya yang rendah, berilium mentransmisikan sinar-X sebanyak 17 kali dan juga aluminium dan telah banyak digunakan dalam pembuatan jendela untuk tabung sinar-X. Berilium dibuat menjadi giroskop, akselerometer, dan komponen komputer untuk instrumen panduan inersia dan perangkat lain untuk rudal, pesawat terbang, dan kendaraan antariksa, dan digunakan untuk drum rem tugas berat dan aplikasi serupa di mana heat sink yang baik adalah penting. Kemampuannya untuk memperlambat neutron cepat telah menemukan aplikasi yang cukup besar dalam reaktor nuklir.
Banyak berilium digunakan sebagai komponen persentase rendah dari paduan keras, terutama dengan tembaga sebagai konstituen utama tetapi juga dengan paduan berbasis nikel dan besi, untuk produk-produk seperti pegas. Berilium-tembaga (2 persen berilium) dibuat menjadi alat untuk digunakan ketika percikan mungkin berbahaya, seperti di pabrik bubuk. Berilium itu sendiri tidak mengurangi percikan, tetapi memperkuat tembaga (dengan faktor 6), yang tidak membentuk percikan api pada saat terjadi benturan. Sejumlah kecil berilium yang ditambahkan ke logam yang teroksidasi menghasilkan lapisan permukaan pelindung, mengurangi sifat mudah terbakar dalam magnesium dan menodai dalam paduan perak.
Neutron ditemukan (1932) oleh fisikawan Inggris Sir James Chadwick ketika partikel dikeluarkan dari berilium yang dibombardir oleh partikel alfa dari sumber radium. Sejak itu berilium dicampur dengan pemancar alfa seperti radium, plutonium, atau amerisium telah digunakan sebagai sumber neutron. Partikel alfa yang dilepaskan oleh peluruhan atom radioaktif bereaksi dengan atom berilium untuk menghasilkan, di antara produk, neutron dengan berbagai energi — hingga sekitar 5 × 10 6 volt elektron (eV). Namun, jika radium dienkapsulasi, sehingga tidak ada partikel alfa yang mencapai berilium, neutron energi kurang dari 600.000 eV dihasilkan oleh radiasi gamma yang lebih penetrasi dari produk peluruhan radium. Contoh penting historis tentang penggunaan sumber berilium / radium neutron termasuk pemboman uranium oleh ahli kimia Jerman Otto Hahn dan Fritz Strassmann dan fisikawan kelahiran Austria Lise Meitner, yang mengarah pada penemuan fisi nuklir (1939), dan pemicunya pada uranium reaksi berantai terkendali pertama oleh fisikawan kelahiran Italia Enrico Fermi (1942).
Satu-satunya isotop yang terjadi secara alami adalah berilium-9 yang stabil, meskipun 11 isotop sintetis lainnya diketahui. Waktu paruh mereka berkisar dari 1,5 juta tahun (untuk berilium-10, yang mengalami peluruhan beta) hingga 6,7 × 10 −17 detik untuk berilium-8 (yang meluruh dengan emisi dua proton). Pembusukan berilium-7 (paruh paruh 53,2 hari) di Matahari adalah sumber neutrino matahari yang diamati.