Fosfor (P), unsur kimia bukan logam dari famili nitrogen (Grup 15 [Va] dari tabel periodik) yang pada suhu kamar berwarna padat, semi transparan, lunak, padatan berlilin yang bersinar dalam gelap.
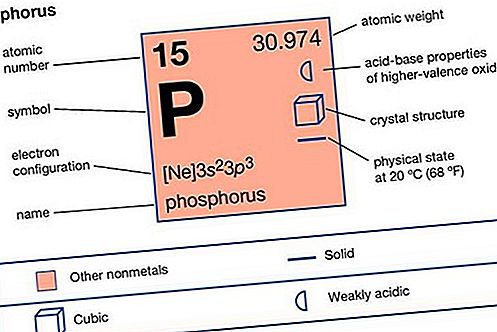
Properti Elemen
| nomor atom | 15 |
|---|---|
| berat atom | 30.9738 |
| titik lebur (putih) | 44.1 ° C (111.4 ° F) |
| titik didih (putih) | 280 ° C (536 ° F) |
| kepadatan (putih) | 1,82 gram / cm 3 pada 20 ° C (68 ° F) |
| keadaan oksidasi | −3, +3, +5 |
| konfigurasi elektron | 1s 2 2s 2 2p 6 3s 2 3p 3 |
Sejarah

Alkemis Arab abad ke-12 mungkin secara kebetulan mengisolasi unsur fosfor, tetapi catatannya tidak jelas. Fosfor tampaknya ditemukan pada 1669 oleh Hennig Brand, seorang pedagang Jerman yang hobinya adalah alkimia. Brand membiarkan 50 ember air seni untuk berdiri sampai membusuk dan “dibiakkan.” Dia kemudian merebus urin menjadi pasta dan memanaskannya dengan pasir, dengan demikian menyaring unsur fosfor dari campuran. Brand melaporkan penemuannya dalam sebuah surat kepada Gottfried Wilhelm Leibniz, dan, setelah itu, demonstrasi elemen ini dan kemampuannya untuk bersinar dalam kegelapan, atau "phosphoresce," menarik minat publik. Fosfor, bagaimanapun, tetap menjadi keingintahuan kimiawi sampai sekitar satu abad kemudian ketika terbukti menjadi komponen tulang. Pencernaan tulang dengan asam nitrat atau asam sulfat membentuk asam fosfat, dari mana fosfor dapat disuling dengan memanaskannya dengan arang. Pada akhir 1800-an James Burgess Readman dari Edinburgh mengembangkan metode tungku listrik untuk memproduksi elemen dari batuan fosfat, yang pada dasarnya adalah metode yang digunakan saat ini.
Distribusi dan kejadian
Fosfor adalah unsur yang sangat banyak didistribusikan — ke-12 yang paling banyak ditemukan di crustEarth's, di mana ia berkontribusi sekitar 0,10 persen berat. Kelimpahan kosmiknya adalah sekitar satu atom per 100 atom silikon, standar. Reaktifitas kimianya yang tinggi memastikan bahwa ia tidak terjadi dalam keadaan bebas (kecuali dalam beberapa meteorit). Fosfor selalu terjadi sebagai ion fosfat. Bentuk gabungan utama di alam adalah garam fosfat. Sekitar 550 mineral berbeda telah ditemukan mengandung fosfor, tetapi, di antaranya, sumber utama fosfor adalah seri apatit di mana ion kalsium ada bersama dengan ion fosfat dan sejumlah variabel ion fluor, klorida, atau hidroksida, sesuai dengan rumus [Ca 10 (PO 4) 6 (F, Cl, atau OH) 2]. Mineral penahan fosfor penting lainnya adalah wavellite dan vivianite. Umumnya, atom logam seperti magnesium, mangan, strontium, dan pengganti timah untuk kalsium dalam mineral, dan silikat, sulfat, vanadat, dan anion serupa menggantikan ion fosfat. Endapan fluoroapatite sedimen yang sangat besar ditemukan di banyak bagian bumi. Fosfat dari tulang dan email gigi adalah hidroksiapatit. (Prinsip mengurangi kerusakan gigi oleh fluoridasi tergantung pada konversi hidroksiapatit menjadi fluoroapatit yang lebih keras dan lebih busuk.)
Sumber komersial utama adalah fosfat, atau batuan fosfat, suatu bentuk masif apatit yang mengandung karbonat. Perkiraan total batuan fosfat dalam kerak bumi rata-rata sekitar 65.000.000.000 ton, di mana Maroko dan Sahara Barat mengandung sekitar 80 persen. Perkiraan ini hanya mencakup bijih yang cukup kaya akan fosfat untuk dikonversi menjadi produk yang bermanfaat dengan metode saat ini. Sejumlah besar material dengan kandungan fosfor yang lebih rendah juga ada.

Satu-satunya isotop fosfor yang terbentuk secara alami adalah isotop massa 31. Isotop lainnya dari massa 24 hingga massa 46 telah disintesis oleh reaksi nuklir yang sesuai. Semua ini adalah radioaktif dengan waktu paruh yang relatif singkat. Isotop massa 32 memiliki paruh 14.268 hari dan telah terbukti sangat berguna dalam studi pelacak yang melibatkan penyerapan dan pergerakan fosfor pada organisme hidup.


![Pertempuran sejarah India Plassey [1757] Pertempuran sejarah India Plassey [1757]](https://images.thetopknowledge.com/img/world-history/5/battle-plassey-indian-history-1757.jpg)





![Pembantaian Srebrenica Sejarah Bosnia [1995] Pembantaian Srebrenica Sejarah Bosnia [1995]](https://images.thetopknowledge.com/img/politics-law-government/4/srebrenica-massacre-bosnian-history-1995.jpg)



