Efusi
Pertimbangkan sistem yang dijelaskan di atas dalam perhitungan tekanan gas, tetapi dengan area A di dinding wadah diganti dengan lubang kecil. Jumlah molekul yang lolos melalui lubang dalam waktu t sama dengan (1/2) (N / V) v z (At). Dalam hal ini, tabrakan antar molekul adalah signifikan, dan hasilnya hanya berlaku untuk lubang kecil di dinding yang sangat tipis (dibandingkan dengan jalur bebas rata-rata), sehingga molekul yang mendekati dekat lubang akan melewati tanpa bertabrakan dengan molekul lain dan dibelokkan. Hubungan antara v z dan kecepatan v rata-rata agak mudah: v z = (1/2) v.
Jika laju untuk dua gas berbeda yang mengalir melalui lubang yang sama dibandingkan, dimulai dengan kerapatan gas yang sama setiap kali, ditemukan bahwa lebih banyak gas ringan yang keluar dari gas berat dan bahwa lebih banyak gas keluar pada suhu tinggi daripada pada suhu rendah., hal lain dianggap sama. Khususnya,
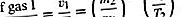
Langkah terakhir mengikuti dari rumus energi, (1/2) mv 2 = (3/2) kT, di mana (v 2) 1/2 diperkirakan menjadi v, meskipun v 2 dan (v̄) 2 sebenarnya berbeda dengan faktor numerik dekat kesatuan (yaitu, 3π / 8). Hasil ini ditemukan secara eksperimental pada tahun 1846 oleh Graham untuk kasus suhu konstan dan dikenal sebagai hukum efusi Graham. Dapat digunakan untuk mengukur berat molekul, untuk mengukur tekanan uap suatu material dengan tekanan uap rendah, atau untuk menghitung laju penguapan molekul dari permukaan cair atau padat.
Transpirasi termal
Misalkan dua wadah dari gas yang sama tetapi pada suhu yang berbeda dihubungkan oleh lubang kecil dan bahwa gas dibawa ke keadaan stabil. Jika lubang cukup kecil dan kerapatan gas cukup rendah sehingga hanya terjadi efusi, tekanan kesetimbangan akan lebih besar pada sisi suhu tinggi. Tetapi, jika tekanan awal pada kedua sisi sama, gas akan mengalir dari sisi suhu rendah ke sisi suhu tinggi untuk menyebabkan tekanan suhu tinggi meningkat. Situasi terakhir disebut transpirasi termal, dan hasil mapan disebut perbedaan tekanan termomolekul. Hasil ini hanya mengikuti dari formula efusi jika hukum gas ideal digunakan untuk menggantikan N / V dengan p / T;
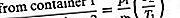
Ketika kondisi mantap tercapai, laju efusi sama, dan dengan demikian
Fenomena ini pertama kali diselidiki secara eksperimental oleh Osborne Reynolds pada 1879 di Manchester, Eng. Kesalahan dapat terjadi jika tekanan gas diukur dalam kapal pada suhu yang sangat rendah atau sangat tinggi dengan menghubungkannya melalui tabung halus ke manometer pada suhu kamar. Sirkulasi gas berkelanjutan dapat diproduksi dengan menghubungkan dua wadah dengan tabung lain yang diameternya besar dibandingkan dengan jalur bebas rata-rata. Perbedaan tekanan mendorong gas melalui tabung ini oleh aliran viskos. Mesin panas yang didasarkan pada aliran sirkulasi ini sayangnya memiliki efisiensi yang rendah.