Properti fisik
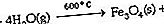
Air memiliki beberapa sifat fisik yang penting. Meskipun sifat-sifat ini akrab karena kehadiran air yang maha besar, sebagian besar sifat fisik air cukup tidak lazim. Mengingat rendahnya massa molar molekul penyusunnya, air memiliki nilai viskositas, tegangan permukaan, panas penguapan, dan entropi penguapan yang luar biasa besar, yang semuanya dapat dianggap berasal dari interaksi ikatan hidrogen yang luas yang terdapat dalam air cair. Struktur terbuka es yang memungkinkan ikatan hidrogen maksimum menjelaskan mengapa air padat kurang padat daripada air cair — situasi yang sangat tidak biasa di antara zat-zat umum.
| Sifat fisik air yang dipilih | |
|---|---|
| masa molar | 18.0151 gram per mol |
| titik lebur | 0,00 ° C |
| titik didih | 100,00 ° C |
| kepadatan maksimum (pada 3,98 ° C) | 1,0000 gram per sentimeter kubik |
| kepadatan (25 ° C) | 0,99701 gram per sentimeter kubik |
| tekanan uap (25 ° C) | 23.75 torr |
| panas fusi (0 ° C) | 6.010 kilojoule per mol |
| panas penguapan (100 ° C) | 40,65 kilojoule per mol |
| panas pembentukan (25 ° C) | −285,85 kilojoule per mol |
| entropi penguapan (25 ° C) | 118,8 joule per ° C mol |
| viskositas | 0,8903 centipoise |
| tegangan permukaan (25 ° C) | 71,97 dynes per sentimeter |
Sifat kimia
Reaksi asam-basa
Air mengalami berbagai jenis reaksi kimia. Salah satu sifat kimiawi air yang paling penting adalah kemampuannya untuk berperilaku sebagai asam (donor proton) dan basa (akseptor proton), sifat khas dari zat amfoter. Perilaku ini paling jelas terlihat dalam autoionisasi air: H 2 O (l) + H 2 O (l) ⇌ H 3 O + (aq) + OH - (aq), di mana (l) mewakili keadaan cair, (aq) menunjukkan bahwa spesies dilarutkan dalam air, dan panah ganda menunjukkan bahwa reaksi dapat terjadi di kedua arah dan kondisi kesetimbangan ada. Pada 25 ° C (77 ° F) konsentrasi H + terhidrasi (yaitu, H 3 O +, yang dikenal sebagai ion hidronium) dalam air adalah 1,0 × 10 -7 M, di mana M mewakili mol per liter. Karena salah satu OH - ion yang diproduksi untuk setiap H 3 O + ion, konsentrasi OH - pada 25 ° C juga 1,0 × 10 -7 M. Dalam air pada 25 ° C H 3 O + konsentrasi dan OH - konsentrasi harus selalu 1,0 × 10 −14: [H +] [OH -] = 1,0 × 10 −14, di mana [H +] mewakili konsentrasi ion H + terhidrasi dalam mol per liter dan [OH -] mewakili konsentrasi OH - ion dalam mol per liter.
Ketika suatu asam (suatu zat yang dapat menghasilkan ion H +) dilarutkan dalam air, baik asam dan air berkontribusi ion H + ke larutan. Ini mengarah pada situasi di mana konsentrasi H + lebih besar dari 1,0 × 10 −7 M. Karena harus selalu benar bahwa [H +] [OH -] = 1,0 × 10 −14 pada 25 ° C, [OH -] harus diturunkan ke beberapa nilai di bawah 1,0 × 10 −7. Mekanisme untuk mengurangi konsentrasi OH - melibatkan reaksi H + + OH - → H 2 O, yang terjadi sejauh yang diperlukan untuk mengembalikan produk [H +] dan [OH -] ke 1,0 × 10 −14 M. Jadi, ketika asam ditambahkan ke air, larutan yang dihasilkan mengandung lebih banyak H + daripada OH -; yaitu, [H +]> [OH -]. Solusi semacam itu (di mana [H +]> [OH -]) dikatakan bersifat asam.
Metode yang paling umum untuk menentukan keasaman suatu larutan adalah pH-nya, yang didefinisikan dalam istilah konsentrasi ion hidrogen: pH = −log [H +], di mana log simbol mewakili logaritma basis-10. Dalam air murni, di mana [H +] = 1,0 × 10 −7 M, pH = 7,0. Untuk larutan asam, pH kurang dari 7. Ketika basa (zat yang berperilaku sebagai akseptor proton) dilarutkan dalam air, konsentrasi H + menurun sehingga [OH -]> [H +]. Solusi dasar ditandai dengan memiliki pH> 7. Singkatnya, dalam larutan air pada 25 ° C:
| solusi netral | [H +] = [OH -] | pH = 7 |
| larutan asam | [H +]> [OH -] | pH <7 |
| solusi dasar | [OH -]> [H +] | pH> 7 |