Pita energi
Logam
Elektron valensi, yang dalam zat lain menghasilkan ikatan antara atom individu atau kelompok kecil atom, dibagi rata oleh semua atom dalam sepotong logam. Elektron-elektron yang terdelokalisasi dengan demikian dapat bergerak di atas seluruh bagian logam dan memberikan kilau logam dan konduktivitas listrik dan termal yang baik dari logam dan paduan. Teori pita menjelaskan bahwa dalam sistem seperti itu, tingkat energi individu digantikan oleh daerah kontinu yang disebut pita, seperti pada diagram kepadatan-keadaan untuk logam tembaga yang ditunjukkan pada gambar. Diagram ini menunjukkan bahwa jumlah elektron yang dapat ditampung dalam pita pada setiap energi yang diberikan bervariasi; dalam tembaga jumlahnya menurun ketika pita mendekati diisi dengan elektron. Jumlah elektron dalam tembaga mengisi pita ke tingkat yang ditunjukkan, meninggalkan ruang kosong pada energi yang lebih tinggi.
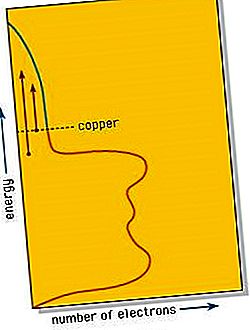
Ketika foton cahaya diserap oleh elektron di dekat bagian atas pita energi, elektron dinaikkan ke tingkat energi yang tersedia lebih tinggi di dalam pita. Cahaya sangat diserap sehingga dapat menembus ke kedalaman hanya beberapa ratus atom, biasanya kurang dari satu panjang gelombang. Karena logam merupakan konduktor listrik, cahaya yang diserap ini, yang merupakan gelombang elektromagnetik, menginduksi arus listrik bolak-balik pada permukaan logam. Arus ini segera mengeluarkan kembali foton dari logam, sehingga memberikan pantulan yang kuat dari permukaan logam yang dipoles.
Efisiensi proses ini tergantung pada aturan seleksi tertentu. Jika efisiensi penyerapan dan reemisi kira-kira sama di semua energi optik, maka warna yang berbeda dalam cahaya putih akan dipantulkan sama baiknya, yang mengarah ke warna "perak" pada permukaan perak dan besi yang dipoles. Dalam tembaga, efisiensi refleksi berkurang dengan meningkatnya energi; berkurangnya reflektifitas pada ujung biru spektrum menghasilkan warna kemerahan. Pertimbangan serupa menjelaskan warna kuning emas dan kuningan.
Semikonduktor murni
Dalam sejumlah zat, celah pita muncul dalam densitas diagram keadaan (lihat gambar). Ini dapat terjadi, misalnya, ketika terdapat rata-rata tepat empat elektron valensi per atom dalam suatu zat murni, menghasilkan pita yang sepenuhnya lebih rendah, yang disebut pita valensi, dan pita atas yang benar-benar kosong, pita konduksi. Karena tidak ada tingkat energi elektron di celah antara dua band, cahaya energi terendah yang dapat diserap sesuai dengan panah A pada gambar; ini mewakili eksitasi elektron dari atas pita valensi hingga ke bawah pita konduksi dan sesuai dengan energi celah pita yang ditunjuk E g. Cahaya dari energi yang lebih tinggi juga dapat diserap, seperti yang ditunjukkan oleh panah B dan C.
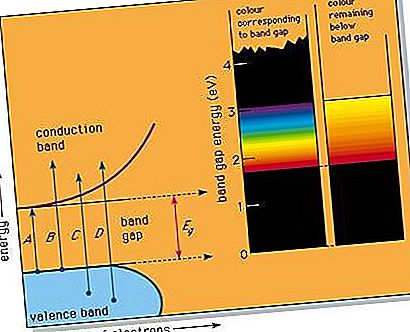
Jika zat memiliki celah pita besar, seperti berlian 5,4 eV, maka tidak ada cahaya dalam spektrum yang terlihat dapat diserap, dan zat tersebut tampak tidak berwarna saat murni. Semikonduktor band-gap besar seperti itu adalah isolator yang sangat baik dan lebih sering diperlakukan sebagai bahan ionik atau ikatan kovalen.
Pigmen cadmium yellow (cadmium sulfide, juga dikenal sebagai mineral greenockite) memiliki celah pita 2,6 eV yang lebih kecil, yang memungkinkan penyerapan ungu dan beberapa warna biru tetapi tidak ada warna lainnya. Ini mengarah ke warna kuningnya. Celah pita yang agak lebih kecil yang memungkinkan penyerapan ungu, biru, dan hijau menghasilkan warna oranye; celah pita yang lebih kecil seperti pada 2.0 eV dari vermilion pigmen (merkuri sulfida, mineral cinnabar) menghasilkan semua energi tetapi merah diserap, yang mengarah ke warna merah. Semua cahaya diserap ketika energi celah pita kurang dari batas 1,77-eV (700-nm) dari spektrum tampak; semikonduktor celah pita sempit, seperti timbal sulfida galena, karenanya menyerap semua cahaya dan berwarna hitam. Urutan warna, kuning, oranye, merah, dan hitam ini adalah kisaran warna yang tepat yang tersedia dalam semikonduktor murni.
Semikonduktor didoping
Jika atom pengotor, sering disebut dopan, hadir dalam semikonduktor (yang kemudian ditetapkan sebagai didoping) dan memiliki jumlah elektron valensi yang berbeda dari atom yang digantikannya, tingkat energi ekstra dapat dibentuk di dalam celah pita. Jika pengotor memiliki lebih banyak elektron, seperti pengotor nitrogen (lima elektron valensi) dalam kristal berlian (terdiri dari karbon, masing-masing memiliki empat elektron valensi), tingkat donor terbentuk. Elektron dari level ini dapat tereksitasi ke dalam pita konduksi oleh penyerapan foton; ini hanya terjadi pada ujung biru spektrum dalam berlian yang diolah nitrogen, menghasilkan warna kuning yang saling melengkapi. Jika pengotor memiliki lebih sedikit elektron daripada atom yang digantikannya, seperti pengotor boron (tiga elektron valensi) dalam berlian, tingkat lubang terbentuk. Foton sekarang dapat diserap dengan eksitasi elektron dari pita valensi ke tingkat lubang. Dalam berlian boron-doped ini hanya terjadi pada ujung kuning spektrum, menghasilkan warna biru tua seperti pada berlian Hope yang terkenal.
Beberapa bahan yang mengandung donor dan akseptor dapat menyerap energi ultraviolet atau listrik untuk menghasilkan cahaya tampak. Misalnya, bubuk fosfor, seperti seng sulfida yang mengandung tembaga dan kotoran lainnya, digunakan sebagai pelapis pada lampu fluoresens untuk mengubah energi ultraviolet yang dihasilkan oleh busur merkuri menjadi cahaya fluoresens. Fosfor juga digunakan untuk melapisi bagian dalam layar televisi, di mana mereka diaktifkan oleh aliran elektron (sinar katoda) di cathodoluminescence, dan dalam cat bercahaya, di mana mereka diaktifkan oleh cahaya putih atau oleh radiasi ultraviolet, yang menyebabkan mereka untuk menampilkan peluruhan bercahaya lambat yang dikenal sebagai fosforensi. Hasil electroluminescence dari eksitasi listrik, seperti ketika bubuk fosfor disimpan ke piring logam dan ditutup dengan elektroda konduksi transparan untuk menghasilkan panel pencahayaan.
Injeksi electroluminescence terjadi ketika kristal berisi persimpangan antara daerah semikonduktor yang berbeda. Arus listrik akan menghasilkan transisi antara elektron dan lubang di wilayah persimpangan, melepaskan energi yang dapat muncul sebagai cahaya hampir monokromatik, seperti pada dioda pemancar cahaya (LED) yang banyak digunakan pada perangkat tampilan dalam peralatan elektronik. Dengan geometri yang cocok, cahaya yang dipancarkan juga bisa monokromatik dan koheren seperti pada laser semikonduktor.













